Chlor ist weniger aggressiv als Fluor, auf
Grund seiner Elektronegativität geht es dennoch viele Verbindungen
ein. Die bekannteste Chlorverbindung ist das Kochsalz (Natriumchlorid),
das bereits in der Antike als Gewürz und Konservierungsmittel (Pökelsalz)
verwendet wurde.
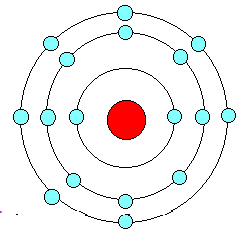
Atombau
|
18 Neutronen(n) Hülle: 17 Elekronen(-) K-Schale: 2
|
 |
Reaktionen des Chlors:
Chlorwasserstoff:
H2 + Cl2 --> 2HCl
Wasserstoff + Chlor --> Chlorwasserstoff(gasf.)
Bildung von Salzsäure:
HCl + H2O --> H3O+ + Cl-
Chlorwasserstoff + Wasser --> Salzsäure
üblicherweise wird HCl
als Salzsäure bezeichnet; Salzsäure ist korrekterweise aber eine
Lösung von Chlorwasserstoff
in Wasser!
Herstellung von Salzsäure aus Kochsalz:
H2SO4 + 2NaCl --> 2HCl + Na2SO4
Schwefelsäure + Natriumchlorid --> Salzsäure + Natriumsulfat
bzw.
H2SO4 + NaCl --> HCl + NaHSO4
Schwefelsäure + Natriumchlorid
--> Salzsäure + Natrihydrogensulfat
Herstellung von Chlor aus Braunstein:
MnO2 + 4HCl --> MnCl2 + 2H2O + Cl2
Mangandioxid + Salzsäure --> Manganchlorid + Wasser + Chlor
Chlor verdrängt die Halogene Brom und Jod aus ihren Verbindungen: (wäßrige Lösung)
2KBr + Cl2 --> 2KCl + Br2
Kaliumbromid + Chlor --> Kaliumchlorid + Brom
2KJ + Cl2 --> 2KCl + J2
Kaliumjodid + Chlor --> Kaliumchlorid + Jod
Weiteres Reaktionsverhalten:
Chlor bildet mit Alkali- und Erdalkalimetallen Salze.
FCKW = Fluorchlorkohlenwasserstoffe sind als Treibgase und Kühlmittel
bekannt geworden. FCKW zerstörten jedoch das Ozon(O3)
in der Ozonschicht unserer Atmosphäre.
![]()
Herstellung von Chlorgas (Cl2)
Versuche, die mit diesem Kennzeichen versehen sind , dürfen nur von fachkundigen
![]()
Personen, bzw. unter deren Aufsicht und Anleitung durchgeführt werden !
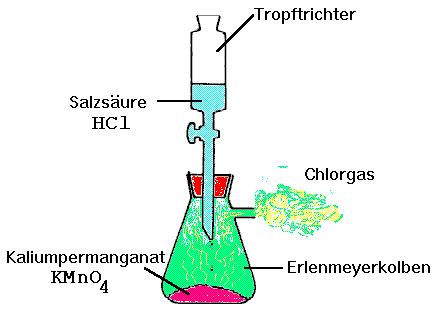
Die Durchführung (s.o.) ist einfach:
Chlorgas ist ein stechend riechendes Gas, das in größeren Mengen gifitg ist. Deshalb für gute Durchlüftung sorgen (ABzug!) MAK-Werte beachten (MAK = maximale Konzentration pro Arbeitsplatz)