
Brom ist weniger aggressiv als Fluor oder Chlor , auf Grund seiner Elektronegativität geht es dennoch viele Verbindungen ein. Bromverbindungen sind als Sedativa und in der Photochemie bekannt geworden.
Atombau
|
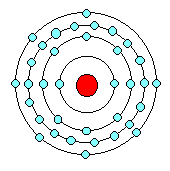
45 Neutronen(n) Hülle: 35 Elekronen(-) K-Schale: 2; L-Schale: 8; M-Schale: 18; N-Schale: 7 |
 |
Reaktionen des Broms:
Bromwasserstoff:
H2 + Br2 --> 2HBr
Wasserstoff + Brom --> Bromwasserstoff(gasf.)
Herstellung von Bromwasserstoff aus Kaliumbromid:
H2SO4 + 2KBr --> 2HBr + K2SO4
Schwefelsäure + Kaliumbromid --> Bromwasserstoff + Kaliumsulfat
bzw.
Schwefelsäure + Kaliumbromid --> Bromwasserstoff + Kaliumhydrogensulfat
Brom verdrängt von den Halogenen nur Jod aus seinen Verbindungen: (wäßrige Lösung)
2KJ + Br2 --> 2KBr + J2
Kaliumjodid + Brom --> Kaliumbromid + Jod
Weiteres Reaktionsverhalten:
Brom bildet mit Alkali- und Erdalkalimetallen Salze.
Organische Bromverbindungen finden z.B. Verwendung als
Schlafmittel. Monobrompropanon wirkt als Tränengas.