Fluor ist eines der aggressivsten und reaktionsfreudigsten chemischen Elemente. Fluor so elektronegativ, daß es sogar Wasser zersetzt und Glas ätzt. Versuche mit Fluorgas oder
Flußsäure(Fluorwasserstoff) bedürfen daher einiger Vorsichtsmaßnahmen.
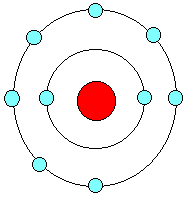
Atombau
|
10 Neutronen(n) Hülle: 9 Elekronen(-) K-Schale: 2; L-Schale: 7 |
 |
Reaktionen des Fluors:
2F2 + 2H2O --> 4HF + O2
Fluor + Wasser --> Fluorwasserstoff + Sauerstoff
3F2 + 2NH3 --> 6HF + N2
Fluor + Ammoniak --> Fluorwasserstoff + Stickstoff
bei der Schmelzflußelektrolyse:
2HF --> H2 + F2
Fluorwasserstoff --> Wasserstoff + Fluor
Bildung von Flußsäure:
HF + H2O --> H3O++ F-
Ätzen von Glas(Quarz):
SiO2+4HF --> SiF4 + 2H2O
Siliziumdioxid + Fluorwasserstoff
-->
Siliziumfluorid + Wasser
Herstellung von Flußsäure aus Flußspat:
H2SO4+CaF2 --> 2HF + CaSO4
Schwefelsäure + Calciumfluorid -->
Flußsäure + Gips
Weiteres Reaktionsverhalten
Fluor bildet mit Alkali- und Erdalkalimetallen Salze. Fluorverbindungen finden Verwendung in Zahnpasta. FCKW = Fluorchlorkohlenwasserstoffe sind als Treibgase und Kühlmittel bekannt geworden. FCKW zerstören das Ozon (O3) in unserer Atmosphäre. Außerdem vertreibt Fluor die anderen Halogene aus ihren Verbindungen.