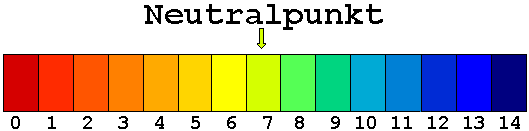
Die Neutralisation
Wenn Säuren mit Laugen reagieren bilden sich Salze und Wasser. Das Entstehen der neutralen Salzlösung kann leicht mit Universalindikator nachgewiesen werden. Während Säuren entsprechend ihrer Stärke den Indikator rötlich färben und die Laugen Blautöne erzeugen führt ihre Neutralisation zum Neutralpunkt(s.Abb.1). Das bei der Neutralisation entstehende Wasser ist weder sauer noch alkalisch und zeigt mit dem handelsüblichen Universalindikator eine typische gelbgrüne Färbung (pH-Wert 7).

Abb. 1: Der Neutralisationspunkt
Das Ergebnis einer Neutralisationsreaktion ist von
den Konzentrationen der verwendeten Säure und Lauge abhängig. Um eine vollständige Neutralisation der beiden Stoffe zu erreichen bedarf es einer quantitativen Neutralisation - der sogenannten »Titration« (Maßanalyse)
![]()
Neutralisation von Natronlauge mit Salzsäure
---- qualitativer Versuch ----
![]()
Versuche, die mit diesem Kennzeichen versehen sind , dürfen nur von fachkundigen
Personen, bzw. unter deren Aufsicht und Anleitung durchgeführt werden.
Arbeitsmittel:
Brenner, Dreifuß, Schutzbrille, Schutzhandschuhe, zwei
Durchführung 1:
Gib in zwei verschiedene Bechergläser je 20 ml konzentrierte Natronlauge und 20 ml konzentrierte Salzsäure. Versetze beide Lösungen mit ein paar Tropfen
------------- Achtung Spritzgefahr! -------------------
Schütte ganz langsam die Salzsäure in die Natronlauge und beobachte die Farbe der Lösung...
------------- Fingerspitzengefühl! --------------------
Wenn die Lösung pH-Wert 7 erreicht hat, kannst du abbrechen...
Beobachtung 1:
Die Farbe des Gemisches ändert sich bei vorsichtiger Vorgehensweise schließlich nach pH 7.
Durchführung 2:
Ein kleiner Teil der neutralen Lösung (nur durchführen wenn pH-Wert 7 erreicht!) wird mit dem Brenner auf einem Dreifuß in einer Porzellanschale eingedampft.
Beobachtung 2:
Es bleibt eine körnige, kristalline Masse zurück, die salzig schmeckt!
Auswertung:
Bei der Reaktion ist Natriumchlorid (Kochsalz) und Wasser entstanden.
NaOH + HCl ---> NaCl + H
2ONatronlauge + Salzsäure ---> Natriumchlorid + Wasser
Hierbei haben die Säurerestionen (Chloridionen) mit den Hydroxidionen der Lauge reagiert:
Na
+ + OH- + H+ + Cl- ---> Na+ + Cl- + H2OOH- = Hydroxidion der Natronlauge;
Cl- = Säurerestion der Salzsäure