 C Ätzend
C Ätzend
Gibt man Alkalimetalle oder Erdalkalimetalle in Wasser, so finden heftige zum Teil sogar sehr heftige Reaktionen statt. Was ist geschehen ? Ein Indikator (Anzeiger für chemische Reaktionen) bringt es ans Licht. Universalindikator zeigt eine Blaufärbung - ein Beweis für das Vorhandensein einer alkalischen Lösung - einer Lauge(Base bzw. Hydroxids)! In der Regel entsteht hierbei zugleich Wasserstoffgas (Reduktion des Wassers), das durch die Knallgasprobe nachgewiesen werden kann.
——————————————————————————————————
Versuche, die mit diesem Kennzeichen versehen sind , dürfen nur von fachkundigen
Personen, bzw. unter deren Aufsicht und Anleitung durchgeführt werden !
——————————————————————————————
Reaktion von Natrium und Wasser
Aufbau: Natrium, Wasser, Phenolphtalein, Spülmittel, Overheadprojektor, Leinwand, Schutzscheibe, Schutzbrille und Handschuhe, Filterpapier,Pinzette, Messer, Glaswanne, Glasstab
Durchführung:
In die Glaswanne wird Wasser gefüllt und mit etwas Spülmittel versetzt damit das Wasser weich wird. Nun kommen noch einige Tropfen Phenolphtalein hinzu und man rührt die Lösung um.
Die Glaswanne wird auf den Overheadprojektor gestellt und die Schutzscheibe darum aufgebaut.
Natrium wird vorsichtig aus der Flasche genommen, vom Petrolium gereinigt und ein max. erbsengroßes Stückchen abgeschintten !
Nun wird das Natriumstückchen auf das Wasser in die Glasschale geworfen. Nach der dem Ende der Reaktion wird umgerührt und der Versuch wiederholt; diesmal wird das Natrium auf einem Filterpapier auf die Wasseroberfläche gesetzt. Vorsicht!!!
Beobachtung:
Das Natrium saust in Form einer kleinen Kugel, so lange bis es sich aufgelöst hat, mit einem zischenden Geräusch unkontrolliert auf der Wasseroberfläche hin und her. Es hinterläßt dabei eine rosafarbene Spur im Wasser.
Bei der Wiederholung des Versuchs mit dem Natrium auf einem Filterpapier entzündet sich das Metall und brennt mit gelboranger Flamme, das Filterpapier brennt jedoch nicht!
Ätzende Dämpfe steigen auf.
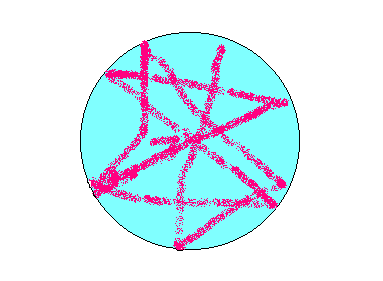
Abb.: Spuren der Reaktion von Natrium und Wasser.
Achtung die folgenden Reaktionen sind zum Teil explosiv....

Alkalimetalle + Wasser:
2Li + 2H2O ---> 2LiOH + H2
Lithium + Wasser ---> Lithiumhydroxid + Wasserstoff
2Na + 2H2O ---> 2NaOH + H2
Natronlauge
Natrium + Wasser ---> Natriumhydroxid + Wasserstoff
2K + 2H2O ---> 2KOH + H2
Kalilauge
Kalium + Wasser ---> Kaliumhydroxid + Wasserstoff
2Rb + 2H2O ---> 2RbOH + H2
Rubidium + Wasser ---> Rubidiumhydroxid + Wasserstoff
2Cs + 2H2O ---> 2CsOH + H2
Lithium + Wasser ---> Lithiumhydroxid + Wasserstoff
---------------------------------------------------------
Hinweis: Auch die Reaktionen von Calcium, Strontium, Barium und heißem bzw. brennendem Magnesium sind gefährlich!
Erdkalimetalle + Wasser:
Be + 2H2O ———> Be(OH)2 + H2
Beryllium + Wasser
———> Berylliumhydroxid + Wasserstoff
Mg + 2H2O ———> Mg(OH) 2 + H2
Magnesium + Wasser
———> Magnesiumhydroxid + Wasserstoff
Kalkwasser
Ca + 2H2O ———> Ca(OH) 2 + H2
Calcium + Wasser
———> Calciumhydroxid + Wasserstoff
Sr + 2H2O ———> Sr(OH)2 + H2
Strontium + Wasser
———> Strontiumhydroxid + Wasserstoff
Barytwasser
Ba + 2H2O ———> Ba(OH)2 + H2
Barium + Wasser
———> Bariumhydroxid + Wasserstoff
Laugen(=wäßrige Hydroxide) bilden Ionen(=elektrisch geladene Teilchen)
Beispiel Calciumhydroxid: Ca(OH)
2
Ca + 2H2O ——> Ca2+ + 2OH- + H2
Die Calciumhydroxidlösung enthält doppelt so viele Hydroxid-Ionen(OH-) wie Calcium-Ionen (Ca2+).